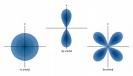
אורביטל
אורביטל- המרחב שבו יש סיכוי (95%) למצוא את האלקטרון במרחב האטום. ישנם מספר סוגי אורביטלים להם צורות מרחביות שונות: s,p,d,f חלוקת האורביטלים לקבוצות היא על פי רמת האנרגיה של אלקטרונים המאכלסים אותו. לאלקטרונים הנמצאים קרוב יותר לגרעין רמת האנרגיה הנמוכה ביותר
כדי לראות אורביטלים באטומים שונים כנס לקישור הבא: אורביטלים באטומים של יסודות שונים
בניסוי דוויסון-גרמר הוכח שאלקטרון מתנהג כמו גל. הדמיה שמציגה את הניסוי:
[ניסוי http://phet.colorado.edu/simulations/sims.php?sim=DavissonGermer_Electron_Diffraction]
על פי עקרון האי-ודאות של הייזנברג אין לדעת בוודעות את מהירות תנועת האלקטרון ואת מיקומו בכל רגע נתון.
קשיים בהוראת הנושא: לתלמידים קשה להבין שאין מסלול בו נע האלקטרוןאו שהמסלול הוא דמיוני. ניתן לדמות את האורביטלים בתוך האטום לאורביטלים של כוכבים במערכת השמש ולשאול:"האם יש מסלול שבו נעים הכוכבם? " תלמידים יכולים להסביר כיצד נקבע מסלול התנועה של כוכב ובכך גם להבין מהו אורביטל של אלקטרון.
עזרי ההוראה: מצגת שבניתי עוזרת להסביר את הערכות האלקטרונים באטום לפי רמות אנרגיה וגם את המושג "אנרגיית יינון"
קישור למצגת: אכלוס אלקטרונים באטום ואנרגיית יינון
דף עבודה בנושא אכלוס אלקטרונים ואנרגיית יינון מדיה:אנרגיית_יינון.doc