קשר יוני: הבדלים בין גרסאות
מתוך Restoeebs Wiki
(ביטול גרסה 481 של גולובצ'יק רוזה (שיחה)) |
|||
| שורה 1: | שורה 1: | ||
= מהו קשר יוני? = | = מהו קשר יוני? = | ||
| − | *קשר | + | *קשר בין שני יונים בעלי מטענים מנוגדים. |
| + | |||
| + | הגדרה מעמיקה יותר למי שלמד על חוזק קשר קוולנטי: | ||
| + | *קשר בין אטומים שונים, הנבדלים במידה רבה בערך האלקטרושליליות שלהם. קשרים אלו "כל-כך" קוטביים עד שיש מעבר של אלקטרון (או אלקטרונים) מאטום אחד (בעל אלקטרושליליות נמוכה) לאטום שני (בעל אלקטרושליליות גבוהה). האטום ש"הפסיד" אלקטרון יהיה בעל מטען חיובי והאטום ש"קיבל" אלקטרון יהיה בעל מטען שלילי. | ||
| + | בין היון חיובי והיון שלילי נוצר קשר כימי שעבורו בנק' איזון מוגדרים אנרגיית קשר ואורך קשר. | ||
*קשר יוני נוצר בין אטומים עם הפרש באלקטרושליליות גדול (מעל 2). | *קשר יוני נוצר בין אטומים עם הפרש באלקטרושליליות גדול (מעל 2). | ||
גרסה מתאריך 06:20, 4 בדצמבר 2009
מהו קשר יוני?
- קשר בין שני יונים בעלי מטענים מנוגדים.
הגדרה מעמיקה יותר למי שלמד על חוזק קשר קוולנטי:
- קשר בין אטומים שונים, הנבדלים במידה רבה בערך האלקטרושליליות שלהם. קשרים אלו "כל-כך" קוטביים עד שיש מעבר של אלקטרון (או אלקטרונים) מאטום אחד (בעל אלקטרושליליות נמוכה) לאטום שני (בעל אלקטרושליליות גבוהה). האטום ש"הפסיד" אלקטרון יהיה בעל מטען חיובי והאטום ש"קיבל" אלקטרון יהיה בעל מטען שלילי.
בין היון חיובי והיון שלילי נוצר קשר כימי שעבורו בנק' איזון מוגדרים אנרגיית קשר ואורך קשר.
- קשר יוני נוצר בין אטומים עם הפרש באלקטרושליליות גדול (מעל 2).
ככל שהפרש באלקטרושליליות הולך וגדל, קוטביות הקשר הולכת וגדלה.
ככל שקשר בין שני אטומים קוטבי יותר, כך גדל מטען החלקי של כל אחד מהאטומים הקשורים.
איזה קשר יווצר בין האטומים עם הפרש בלקטרושליליות גדול מאוד? כגון, בין אטום נתרן לבין אטום כלור שהפרש בלקטרושליליות הוא 2.1?
במקרה כזה הקשר הוא כל-כך קוטבי, שניתן לומר שהאלקטרון הערכי השייך לאטום נתרן עובר לאטום כלור. כתוצאה מכך נוצר זוג יונים:
יון כלור שלילי -Cl יון נתרן חיובי +Na
דוגמאות נוספות
בין פלואור וליתיום קיים קשר יוני (הפרש באלקטרושליליות שווה ל-3) שבו יש יוני F- ויוני Li+.
מה אופייני לקשר יוני?
- על פי חוק קולון, ניתן להסיק כי הקשרים בין זוג יונים (כמו בין הפלואור לליתיום) יהיו די חזקים, כיוון שהמטענים החשמליים גדולים יחסית.
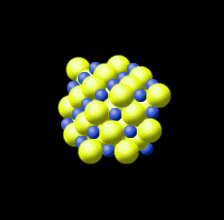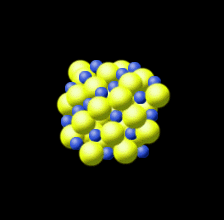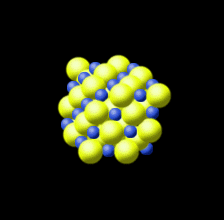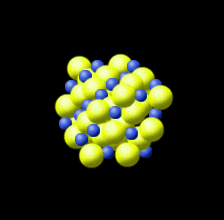
- לתרכובות יוניות יש מבנה ענק של יונים חיוביים ושליליים.
- יונים חיוביים ושלילים מתנדדים בשריג היוני (ראה מודל באנימצייה)
ההסבר: ככל שיוני כלור ונתרן רבים יותר קשורים זה לזה במבנה אחד, כך החלקיק יציב יותר.