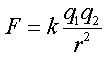קשרים בין מולקולריים: הבדלים בין גרסאות
| שורה 41: | שורה 41: | ||
==מאפייני האינטראקציה== | ==מאפייני האינטראקציה== | ||
| + | |||
| + | האינטראקציות בין הצורונים גורמות לעוות האורביטלים המולקולריים של הצורונים , לשינוי חופש תנועתם , לשינוי האנרגיה הפוטנציאלית של הצורונים ולשינוי המרחק בין מרכזי הצורונים . | ||
| + | המאפיינים האנרגיה הפוטנציאלית והמרחק בין הצורונים נתנים למדידה וחישוביםכמותיים והם הבסים לסיווג הקשרים הבין מולקולריים . | ||
=סיווג הקשרים הבין-מוליקולריים= | =סיווג הקשרים הבין-מוליקולריים= | ||
גרסה מתאריך 01:41, 8 בדצמבר 2009
חומר בצובר מורכב ממספרים עצומים של חלקיקים : אטומים , מולקולות , יונים ( שם כולל - צורונים ) . הצורונים השונים ( בגודלם , בצורותם ובקוטביות שלהם ) נמצאים בצובר באינטראקציות שונות . לאינטראקציות בין הצורונים בצובר נהוג לקרוא כוחות בין מולקולריים ( intermolecular forces ) - הכוחות הפועלים בין המולקולות , להבדיל מהכוחות האחראים להיווצרות קשרים כימיים בין האטומים - הקשרים הכימיים הנובעים מהכוחות התוך מולקולריים ( intramolecular forces ) . הכוחות הבין מולקולריים קושרים את הצורונים זה לזה בצובר והם בעלי חשיבות מכרעת בקביעת התכונות הפיזיקליות של חומר בצובר , לכן השם הנוסף של הכוחות הבין מולקולריים הוא קשרים בין מולקולריים .
הערה :
חומר בצובר ( bulk matter ) - כמות מסוימת של חומר שתכונותיו נובעות מתכונות הצורונים , המרכיבים את כל אחד ממצבי צבירה של החומר ( מוצק , נוזל , גז ) .
תוכן עניינים
סוגי הקשרים הבין מולקולריים
קיימים הקשרים הבין מולקולרים השונים : כוחות ואן דר ואלס ( כוחות לונדון ) - בין מולקולות לא קוטביות או בין מולקולות לא קוטביות לבין מולקולות קוטביות , כוחות בין מולקולות קוטביות , קשרי מימן , כוחות בין יון לבין מולקולות קוטביות .
נתן להסביר את מקור הקשרים הבין מולקולריים השונים על פי חוק קולון , המתאר את את האינטראקציות בין הצורונים השונים .
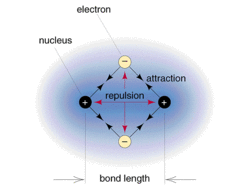
כל הצורונים נמשכים זה לזה כשהן במרחק של כמה רדיאוסים מולקולריים , אך דוחים זה את זה מייד כאשר ענני האלקטרוניים שלהם באים במגע. כתוצאה , משתנה האנרגיה הפוטנציאלית של הצורון כתלות במרחק מהצורון האחר . במרחקים בינוניים האנרגיה הפוטנציאלית נמוכה מאשר במרחק אינסופי. משיכה מורידה תמיד את האנרגיה הפוטנציאלית של הצורונים. כאשר נוצר מגע בין הצורונים האנרגיה הפוטנציאלית מתחילה לעלות , שכן דחייה מעלה תמיד את האנרגיה הפוטנציאלית של הצורונים . כאשר על הצורונים לא פועלים כוחות נוספים , כוחות המשיכה והדחייה בין הצורונים משתווים וכתוצאה הצורונים נצמדים זה לזה במרחק מסוים - נוצרו הקשרים הבין מולקולריים .
בין אלו הצורונים עשויות להתקיים האינטראקציות השונות ?
כל האינטראקציות בין הצורונים הן אינטראקציות קולוניות בין שני מטענים . הצורונים שונים זה מזה בקוטביות שלהם , לכן נוצרים סוגים שונים של האינטראקציות :
סוגי האינטראקציות :
1. אינטראקציות דיפול מושרה - דיפול מושרה : הצורונים המעורבים - כל סוגי המולקולות .
2. אינטראקציות דיפול - דיפול מושרה : הצורונים המעורבים - אחת המולקולות לפחות צריכה להיות קוטבית .
3. אינטראקציות דיפול - דיפול : הצורונים המעורבים - מולקולות קוטביות נייחות או מסתחררות .
4. קשרי מימן : הצורונים המעורבים - מולקולות המכילות אטום מימן הקשור בקשר קוולנטי לאטום N , O , F .
5. אינטראקציות יון - דיפול : הצורונים המעורבים - יונים ומולקולות קוטביות .
מאפייני האינטראקציה
האינטראקציות בין הצורונים גורמות לעוות האורביטלים המולקולריים של הצורונים , לשינוי חופש תנועתם , לשינוי האנרגיה הפוטנציאלית של הצורונים ולשינוי המרחק בין מרכזי הצורונים . המאפיינים האנרגיה הפוטנציאלית והמרחק בין הצורונים נתנים למדידה וחישוביםכמותיים והם הבסים לסיווג הקשרים הבין מולקולריים .
סיווג הקשרים הבין-מוליקולריים
אינטראקציות ון דר ולס
אינטראקציות דיפול דיפול
הצעות לתירגול
קישורים חיצוניים