אורביטל: הבדלים בין גרסאות
| שורה 10: | שורה 10: | ||
על כל אורביטל יכולים לנוע שני אלקטרונים בעלי כיוני תנועה ( ספין)מנוגדים | על כל אורביטל יכולים לנוע שני אלקטרונים בעלי כיוני תנועה ( ספין)מנוגדים | ||
באטומים עם רמות אנרגיה גבוהות אלקטרונים מאכלסים קודם את האורביטל בעלת אנרגיה נמוכה ברמה גבוהה יותר ורק אחר כך אורביטלים ברמה נמוכה יותר. | באטומים עם רמות אנרגיה גבוהות אלקטרונים מאכלסים קודם את האורביטל בעלת אנרגיה נמוכה ברמה גבוהה יותר ורק אחר כך אורביטלים ברמה נמוכה יותר. | ||
| − | באיור ניתן לראות | + | באיור ניתן לראות שלאורביטלים 3d אנרגיה גבוהה יותר מאורביטלים 4s ן-4p|. |
[[תמונה:רמות אנרגיה באטום וסוגי האורביטלים2.gif]] | [[תמונה:רמות אנרגיה באטום וסוגי האורביטלים2.gif]] | ||
| שורה 17: | שורה 17: | ||
[http://www.orbitals.com/orb/orbtable.htm אורביטלים באטומים של יסודות שונים] | [http://www.orbitals.com/orb/orbtable.htm אורביטלים באטומים של יסודות שונים] | ||
| − | בניסוי דוויסון-גרמר הוכח | + | בניסוי דוויסון-גרמר הוכח ש[[אלקטרון]] מתנהג כמו גל. |
הדמיה שמציגה את הניסוי: | הדמיה שמציגה את הניסוי: | ||
גרסה מתאריך 13:39, 29 בנובמבר 2009
אורביטל- המרחב שבו יש סיכוי (95%) למצוא את האלקטרון במרחב האטום.
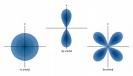
ישנם מספר סוגי אורביטלים להם צורות מרחביות שונות: s,p,d,f
אלקטרונים באטום נמצאים ברמות אנרגיה שונות. רמת אנרגיה יכולה להכיל מספר אורביטלים שונים. על כל אורביטל יכולים לנוע שני אלקטרונים בעלי כיוני תנועה ( ספין)מנוגדים באטומים עם רמות אנרגיה גבוהות אלקטרונים מאכלסים קודם את האורביטל בעלת אנרגיה נמוכה ברמה גבוהה יותר ורק אחר כך אורביטלים ברמה נמוכה יותר. באיור ניתן לראות שלאורביטלים 3d אנרגיה גבוהה יותר מאורביטלים 4s ן-4p|.
קובץ:רמות אנרגיה באטום וסוגי האורביטלים2.gif
כדי לראות אורביטלים באטומים שונים כנס לקישור הבא: אורביטלים באטומים של יסודות שונים
בניסוי דוויסון-גרמר הוכח שאלקטרון מתנהג כמו גל. הדמיה שמציגה את הניסוי:
[ניסוי http://phet.colorado.edu/simulations/sims.php?sim=DavissonGermer_Electron_Diffraction]
על פי עקרון האי-ודאות של הייזנברג אין לדעת בוודעות את מהירות תנועת האלקטרון ואת מיקומו בכל רגע נתון ולכן משתמשים במושג אורביטל המתאר את המקום האפשרי להמצאותו של אלקטרון במרחב.
קשיים בהוראת הנושא: לתלמידים קשה להבין שאין מסלול בו נע האלקטרוןאו שהמסלול הוא דמיוני. ניתן לדמות את האורביטלים בתוך האטום לאורביטלים של כוכבים במערכת השמש ולשאול:"האם יש מסלול שבו נעים הכוכבם? " תלמידים יכולים להסביר כיצד נקבע מסלול התנועה של כוכב ובכך גם להבין מהו אורביטל של אלקטרון.
עזרי ההוראה: מצגת שבניתי עוזרת להסביר את הערכות האלקטרונים באטום לפי רמות אנרגיה וגם את המושג "אנרגיית יינון"
קישור למצגת: אכלוס אלקטרונים באטום ואנרגיית יינון
דף עבודה בנושא אכלוס אלקטרונים ואנרגיית יינון מדיה:אנרגיית_יינון.doc