אורביטל: הבדלים בין גרסאות
| שורה 40: | שורה 40: | ||
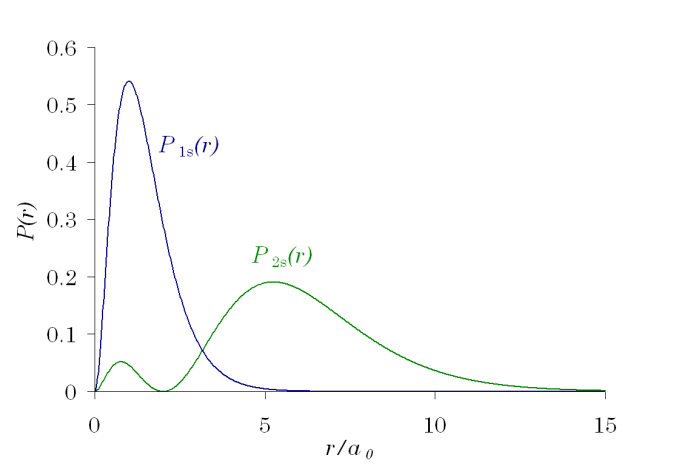
גרף שלפניכם מציג את ----------------------. | גרף שלפניכם מציג את ----------------------. | ||
| − | אלקטרונים המאכלסים את האורביטלים 2s ו- | + | אלקטרונים המאכלסים את האורביטלים 2s ו-2s נמצאים במרחק שונה מהגרעין וסבירות-------------. |
[[תמונה:Fig3.png]] | [[תמונה:Fig3.png]] | ||
גרסה מתאריך 18:43, 5 בינואר 2010
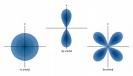
אורביטל- המרחב סביב גרעין שבו יש סיכוי גדול למצוא את האלקטרון במרחב האטום. לפי מכניקה קוונטית האורביטל מאפיין גם את האנרגיה שיש לאלקטרון במצב יציב(לא מעורר) וגם צורתו של ענן האלקטרוני במרחב.
באיור ניתן לראות את צורה המרחבית של אורביטלים מסוג s (ספרי) ומסוג p (שמיניה תלת-מימדית)
הצגה כזאת של אורביטלים מקובלת בהרבה ספרי לימוד, אך היא יכולה להיות מקור לתפיסה שגויאה שאלקטרון נע במסלול מוגדר.
אורביטל הוא מכלול של כל התנועות המורכבות של אלקטרון.
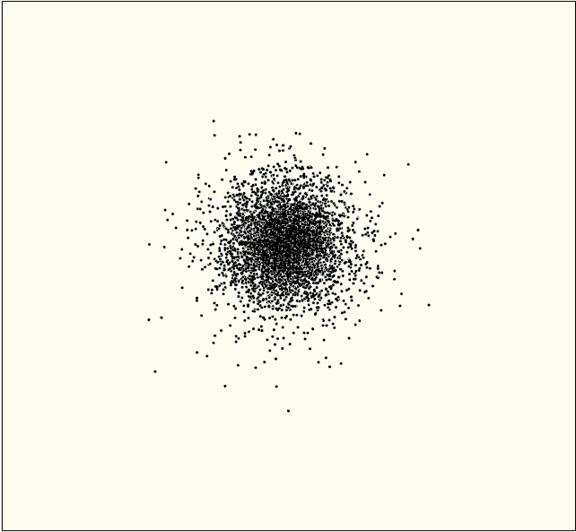
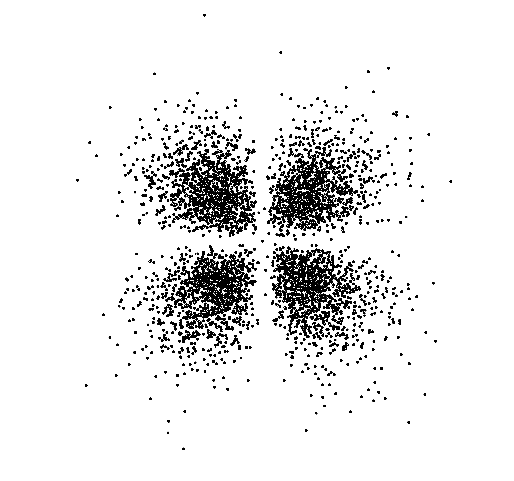
איור הבא מציג את האורביטל בצורה נכונה יותר: נקודות מסמלות את המקומות האפשריות בהם יכול להמצא האלקטרון. באזור בו צפיפות הנקודות גבוהה יותר יש סיכוי רב יותר להמצאות האלקטרון.
תכונת הגל של אלקטרון קובעת את סוג האורביטל
במכניקה קוונטית מצבו של אלקטרון במרחב תלת-מימדי מתואר על ידי משוואת שרדינגר (שנת 1926 )
פתרון של משוואה זאת נותן פונקציה גלית (Ψ=f(x, y, z
שמאפשרת להעריך את סיכוי למציאת האלקטרון במרחב מסויים סביב הגרעין
משוואת שרדינגר מאפשרת לאפיין התנהגות של כל אלקטרון באטום על ידי שלושה מספרים קוונטים: n,l,m
לפי חישובים של מכניקה קוונטית אורביטלים שונים גם בגודל וגם בצורה המרחבית שלהם
ישנם מספר סוגי אורביטלים להם צורות מרחביות שונות: s,p,d,f
כדי לראות אורביטלים שונים כנס לקישור הבא: [1]
בכל אורביטל יכולים להימצא שני אלקטרונים בעלי כיוני תנועה סיבובית (ספין) מנוגדים.
גרף שלפניכם מציג את ----------------------.
אלקטרונים המאכלסים את האורביטלים 2s ו-2s נמצאים במרחק שונה מהגרעין וסבירות-------------.
באטומים עם מספר גדול של אלקטרונים הם מאכלסים קודם את האורביטל